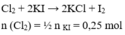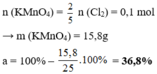Những câu hỏi liên quan
Câu 1: Để mẩu giấy quỳ tím ẩm vào bình khí clo một thời gian. Nêu hiện tượng và giải thích.Câu 2: Cho m gam KMnO4 tác dụng hết với dung dịch HCl (đặc) dư, toàn bộ khí clo sinh ra tác dụng hết với Fe dư, thu được 16,25 gam FeCl3. Tính số mol HCl phản ứng và giá trị m.Câu 3: Hòa tan m gam hỗn hợp X gồm Fe và Cu vào dung dịch HCl 2M (lấy dư 10% so với lượng cần dùng) sau phản ứng thu được 4,48 lít khí (đktc). Mặt khác, đốt cháy m gam X trong khí clo dư thu được 48,7g hỗn hợp muối.a) Viết các phương...
Đọc tiếp
Câu 1: Để mẩu giấy quỳ tím ẩm vào bình khí clo một thời gian. Nêu hiện tượng và giải thích.
Câu 2: Cho m gam KMnO4 tác dụng hết với dung dịch HCl (đặc) dư, toàn bộ khí clo sinh ra tác dụng hết với Fe dư, thu được 16,25 gam FeCl3. Tính số mol HCl phản ứng và giá trị m.
Câu 3: Hòa tan m gam hỗn hợp X gồm Fe và Cu vào dung dịch HCl 2M (lấy dư 10% so với lượng cần dùng) sau phản ứng thu được 4,48 lít khí (đktc). Mặt khác, đốt cháy m gam X trong khí clo dư thu được 48,7g hỗn hợp muối.
a) Viết các phương trình phản ứng xảy ra
b) Tính m và phần trăm khối lượng của Cu trong hỗn hợp X
c) Tính thể tích dung dịch HCl đã dùng
Câu 2 :
\(n_{FeCl_3} = \dfrac{16,25}{162,5} = 0,1(mol)\)
2Fe + 3Cl2 \(\xrightarrow{t^o}\) 2FeCl3
0,1......0,15.........0,1.................(mol)
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,06.............0,48...................................0,15....................(mol)
Suy ra :
m = 0,06.158 = 9,48(gam)
\(m_{HCl} = 0,48.36,5 = 17,52(gam)\)
Đúng 2
Bình luận (0)
Giải thích các bước giải:
1. khi chó khí clo vào giấy quỳ ẩm thì ngay lập tức clo tác dụng vs nc đk ánh sáng sẽ tạo thành HCL ==> quỳ chuyển đỏ vì HCl là ãit
Đúng 2
Bình luận (0)
Câu 1 : Ban đầu quỳ tím hóa đỏ (do có HCl), sau đó quỳ tím mất màu do tính oxi hóa mạnh của HClO
Cl2 + H2O ⇌ HCl + HClO
Đúng 0
Bình luận (0)
Đun nóng 22,12 gam KMnO4 thu được 21,26 gam hỗn hợp rắn. Cho hốn hợp rắn tác dụng với dung dịch HCl đặc thì lượng khí clo thoát ra là (hiệu suất phản ứng 100%) A. 0,17 mol. B. 0,49 mol. C. 0,26 mol. D. 0,29 mol.
Đọc tiếp
Đun nóng 22,12 gam KMnO4 thu được 21,26 gam hỗn hợp rắn. Cho hốn hợp rắn tác dụng với dung dịch HCl đặc thì lượng khí clo thoát ra là (hiệu suất phản ứng 100%)
A. 0,17 mol.
B. 0,49 mol.
C. 0,26 mol.
D. 0,29 mol.
Cho 25 gam K M n O 4 (có a% tạp chất) tác dụng với dung dịch HCl dư thu được khí clo. Để khí clo sinh ra phản ứng vừa đủ với dung dịch chứa 83 gam KI tạo I 2 , giá trị của a là
A. 20
B. 59,25
C. 36,8
D. 26
Cho m gam Hiđrocarbon no, mạch vòng A tác dụng với khí clo (chiếu sáng) thu được 9,48 g một dẫn suất clo duy nhất B. Để trung hòa khí HCl sinh ra cần vừa đúng 80ml dung dịch NaOH 1M. Hiệu suất clo hóa là 80%. Giá trị của m bằng A. 8,4 g B. 6,72 g C. 5,376 g D. 7,5 g
Đọc tiếp
Cho m gam Hiđrocarbon no, mạch vòng A tác dụng với khí clo (chiếu sáng) thu được 9,48 g một dẫn suất clo duy nhất B. Để trung hòa khí HCl sinh ra cần vừa đúng 80ml dung dịch NaOH 1M. Hiệu suất clo hóa là 80%. Giá trị của m bằng
A. 8,4 g
B. 6,72 g
C. 5,376 g
D. 7,5 g
Cho m gam KMnO4tác dụng hết với dung dịch HCl (đặc) dư, toàn bộ khí clo sinh ra tác dụng hết với Fe dư, thu được 16,25 gam FeCl3. Tính số mol HCl phản ứng và giá trị m
Đọc tiếp
Cho m gam KMnO4tác dụng hết với dung dịch HCl (đặc) dư, toàn bộ khí clo sinh ra tác dụng hết với Fe dư, thu được 16,25 gam FeCl3. Tính số mol HCl phản ứng và giá trị m
Đốt cháy m gam Fe trong khí Clo thu được chất rắn A. Hoà tan A vào nước dư thu được dung dịch B và 2,8 gam chất rắn không tan. Cho B tác dụng với lượng dư dung dịch KMnO4 trong môi trường H2SO4, thì thấy có 0,18 mol KMnO4 tham gia phản ứng. Phần trăm khối lượng Fe tham gia phản ứng với Clo là
Mọi người giúp e với ạ...e cảm ơn
\(Fe^{2+} \to Fe^{3+} + 1e\\ Mn^{+7} + 5e \to Mn^{2+}\\ \Rightarrow n_{Fe^{2+}} = 5n_{KMnO_4} = 0,18.5 =0,9(mol)\\ 2FeCl_3 + Fe \to 3FeCl_2\\ n_{FeCl_3} = \dfrac{2}{3}n_{FeCl_2} = 0,6(mol)\\ n_{Fe\ pư} = \dfrac{1}{3}n_{Fe} = 0,3(mol)\\ \Rightarrow m_{Fe\ trong\ A} = 2,8 + 0,3.56 = 19,6(gam)\\ 2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Fe} = n_{FeCl_3} = 0,6(mol)\\\)
Phần trăm khối lượng Fe tham gia phản ứng là : \(\dfrac{0,6.56}{0,6.56 + 19,6}.100\% = 63,15\%\)
Đúng 2
Bình luận (1)
nung nóng 22,12 gam KMnO4 và 18,375 gam KClO3, sau một thời gian thu được chất rắn X gồm 6 chất có khối lượng 37,295 gam. Cho X tác dụng với dung dịch HCl đặc dư, đun nóng. Toàn bộ lượng khí clo thu được cho phản ứng hết với m gam bột Fe đốt nóng được chất nóng Y. Hòa tan hoàn toàn Y vào nước được dung dịch Z. thêm AgNO3 dư vào dung dịch Z đến khi phản ứng hoàn toàn được 204,6 gam kết tủa. Giá trị m là A. 22,44 B. 28,0 C. 33,6 D. 25,2
Đọc tiếp
nung nóng 22,12 gam KMnO4 và 18,375 gam KClO3, sau một thời gian thu được chất rắn X gồm 6 chất có khối lượng 37,295 gam. Cho X tác dụng với dung dịch HCl đặc dư, đun nóng. Toàn bộ lượng khí clo thu được cho phản ứng hết với m gam bột Fe đốt nóng được chất nóng Y. Hòa tan hoàn toàn Y vào nước được dung dịch Z. thêm AgNO3 dư vào dung dịch Z đến khi phản ứng hoàn toàn được 204,6 gam kết tủa. Giá trị m là
A. 22,44
B. 28,0
C. 33,6
D. 25,2
Chọn đáp án B
Ta có
![]()
=0,2
![]()
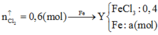
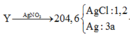
![]()
=>a=0,1(mol)
![]()
Đúng 0
Bình luận (0)
Cần bao nhiêu gam KMnO4 và bao nhiêu ml dung dịch HCl 1M để điều chế đủ khí Clo tác dụng với Fe tạo nên 16,25 gam FeCl3 ?
Xem chi tiết
\(n_{FeCl_3}=\dfrac{16.25}{162.5}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(......0.15......0.1\)
\(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\)
\(0.06...............0.48........................................0.15\)
\(m_{KMnO_4}=0.06\cdot158=9.48\left(g\right)\)
\(V_{dd_{HCl}}=\dfrac{0.48}{1}=0.48\left(l\right)=480\left(ml\right)\)
Đúng 3
Bình luận (2)
\(2Fe+ 3Cl_2 \xrightarrow{t^o} 2FeCl_3\\ n_{Cl_2} = \dfrac{3}{2}n_{FeCl_3} = \dfrac{3}{2}.\dfrac{16,25}{162,5} = 0,15(mol)\\ 2KMnO_4 + 16HCl \to 2KCl + 2MnCl_2 + 5Cl_2 + 8H_2O\\ n_{KMnO_4} = \dfrac{2}{5}n_{Cl_2} = 0,06(mol)\\ \Rightarrow m_{KMnO_4} = 0,06.158 = 9,48(gam)\\ n_{HCl} = \dfrac{16}{4}n_{Cl_2} = 0,48(mol)\\ \Rightarrow V_{dd\ HCl} = \dfrac{0,48}{1} = 0,48(lít) = 480(ml)\)
Đúng 1
Bình luận (0)
Đốt nóng một hỗn hợp gồm 5,6 gam bột Fe và 1,6 gam bột S trong môi trường không có không khí, thu được hỗn hợp rắn X. Cho hỗn hợp khí tác dụng hoàn toàn với 500ml dung dịch HCl, thu được hỗn hợp khí A và dung dịch B ( hiệu suất phản ứng đạt 100% )a) Tính thành phần phần trăm theo thể tich của hỗn hợp Ab) Biết rằng cần dùng 125ml dung dịch NaOH 0,1M để trung hòa HCl còn dư trong dung dịch B, hãy tính nồng độ của dung dịch HCl đã dùng
Đọc tiếp
Đốt nóng một hỗn hợp gồm 5,6 gam bột Fe và 1,6 gam bột S trong môi trường không có không khí, thu được hỗn hợp rắn X. Cho hỗn hợp khí tác dụng hoàn toàn với 500ml dung dịch HCl, thu được hỗn hợp khí A và dung dịch B ( hiệu suất phản ứng đạt 100% )
a) Tính thành phần phần trăm theo thể tich của hỗn hợp A
b) Biết rằng cần dùng 125ml dung dịch NaOH 0,1M để trung hòa HCl còn dư trong dung dịch B, hãy tính nồng độ của dung dịch HCl đã dùng
`a)`
`n_{Fe}=0,1(mol);n_S=0,05(mol)`
`S+Fe` $\xrightarrow{t^o}$ `FeS`
`0,05->0,05->0,05(mol)`
`0,1>0,05->Fe` dư.
`->X` gồm `Fe:0,1-0,05=0,05(mol);FeS:0,05(mol)`
`Fe+2HCl->FeCl_2+H_2`
`FeS+2HCl->FeCl_2+H_2S`
Theo PT: `n_{H_2}=n_{Fe}=0,05(mol);n_{H_2S}=n_{FeS}=0,05(mol)`
`->\%V_{H_2}=\%V_{H_2S}={0,05}/{0,05+0,05}.100\%=50\%`
`b)`
`n_{NaOH}=0,125.0,1=0,0125(mol)`
`NaOH+HCl->NaCl+H_2O`
Theo PT: `\sum n_{HCl}=n_{NaOH}+2n_{H_2}+2n_{H_2S}=0,2125(mol)`
`->C_{M\ HCl}={0,2125}/{0,5}=0,425M`
Đúng 2
Bình luận (0)